iyon, anyon ve katyon
Yüklü atom veya atom gruplarına
iyon denir. (+) yüklü iyonlara
katyon, (-) yüklü iyonlara da
anyon denir. Katyonlar +1, +2, +3 ve +4 yüklü olabilir. Anyonlar da -1, -2 ve -3 yüklü olabilir. Anyon ve katyonların listesini kitaplarınızdan bulabilirsiniz. Bunların bilinmesi gerekir. Bileşik formülleri yazılırken,önce (+) yüklü iyon, sonrada (-) yüklü iyon yazılır.
Örnek:
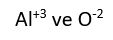
iyonlarından oluşan bileşiğin formülü yazılırken üstteki sayılar çapraz bir şekilde diğerinin altına getirilir.
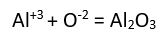
şeklinde yazılır.
Katyonun adı + Anyonun adı = Bileşiğin adı 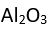
(Alüminyum oksit)
Bileşikler içlerindeki elementlerin türlerine göre; Metal-Metal bileşikleri ve Ametal -ametal bileşikleri olarak ikiye ayrılır. Adlandırmaları da birbirinden farklı olur. Örneğin; yukarıdaki
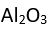
bileşiği metal-ametal bileşiklerine bir örnektir. Bir bileşiğin moleküllerindeki atomlar ve bunların sayıları farklı şekilde gösterilebilir.Molekül şekil olarak modellerle gösterilebileceği gibi açık, yarı açık ve kapalı formüllerle de gösterilebilir. Açık formüllere yarı formülde denir. Bunlara atomların birbiriyle yaptıkları bağlar da belirtilebilmektedir. Fakat reaksiyon kimyasında daha çok kapalı formül kullanılır.

yazılışında atomların ad ve sayıları belirtilmiştir.

molokülü bir alüminyum ve 3 adet klor atomundan oluşur.
Kaba formülle molekül formülü arasındaki farkın anlaşılmasında yarar vardır. Kaba formül sadece, bileşiği oluşturan elementlerin bileşikteki bağıl atom sayıları arasındaki oranı gösterir. Fakat gerçekte bileşiğin moleküllerinde kaçar atom bulunduğunu ifade etmez. Molekül formülü ise bileşiğin molekülündeki atomların gerçek sayısını gösterir. Gerçek formül veya kimyasal formül diye de adlandırılır.